
Transport nucléocytoplasmique et intranucléaire des virus et médiateurs de l’immunité
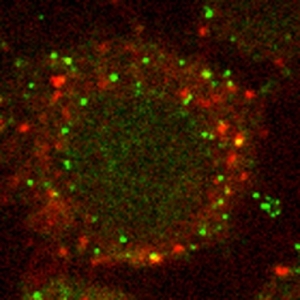
Les virus qui se répliquent dans le noyau (comme le VIH et le virus de la grippe) dépendent du complexe du pore nucléaire (« Nuclear pore complex », ou NPC) et de l’architecture nucléaire pour la réplication de leur génome, qui peut persister dans le noyau cellulaire sous forme de cassette intégrée dans la chromatine, d’épisomes ou d’entités génomiques complexes.
Les NPC peuvent favoriser la réplication virale en offrant un micro-environnement riche en nucléotides, en composants de la machinerie SUMO (comme RanBP2, RanGAP1, Ubc9, SENP2), ainsi qu’un réseau hautement connecté avec le cytosquelette et l’architecture nucléaire. Toutefois, les NPC sont également des modulateurs clés dans la réponse antivirale, puisqu’ils régulent l’import de facteurs de transcription de l’immunité innée (les protéines IRF ou NF-κB, notamment) et de facteurs antiviraux (comme TRIM5α) ainsi que l’export de transcrits codant pour des cytokines (par exemple l’ARNm de l’IL-6). De même, des organelles sans membrane du noyau tels que les corps nucléaires de PML (PML-NB) peuvent contrôler l’expression du génome viral et l’établissement de la latence, mais constituent également un point névralgique de la défense antivirale.
C’est la nature centrale des NPC et d’autres structures nucléaires dans la réplication virale et l’immunité innée qui anime nos projets de recherche.
 |
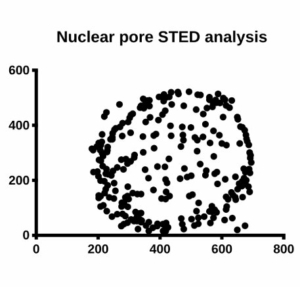
Projet 1 : Transport du VIH vers le noyau et translocation nucléaire. Depuis plusieurs années, notre équipe étudie en profondeur les mécanismes qui sous-tendent l’import nucléaire et la décapsidation du VIH. Nous avons récemment identifié un signal de localisation nucléaire atypique dans la capside du VIH-1 qui est reconnu par la Transportine-1 pour accompagner les capsides du VIH-1 à travers les NPC. Nous développons actuellement des inhibiteurs d’interaction Transportine-1/capside qui agissent comme des antiviraux spécifiques de l’import nucléaire avec une efficacité élevée et une faible toxicité. |
 |
Projet 2 : Contrôle de la réponse immunitaire innée à l’infection grippale par RanBP2. RanBP2 est un composant des fibrilles cytoplasmiques des NPC. Nous avons déjà étudié son importance dans l’arrimage du VIH-1 au NPC ainsi que dans la modulation des fonctions de TRIM5α dans les cellules dendritiques. Nos recherches portent actuellement sur la façon dont RanBP2 module la production de cytokines pro-inflammatoires à la suite d’une infection par le virus Influenza A, et comment ce processus est perturbé dans la maladie génétique rare qu’est l’encéphalopathie nécrosante aiguë (ANE1). |
L’équipe VTRIS:

L’équipe en Avril 2024
A l’arrière, de gauche à droite: S. Nisole, G. Beucher, I. Bribes, R. Gaye, S. Desgraupes, M. Gonzalez, M. Seite, A. Decorsière. A l’avant, de gauche à droite: J. Zoladek, S. Perrin, M. Cannac, N. Arhel

L’équipe en Avril 2023
De gauche à droite: S. Nisole, T. Léocadie, A. Decorsière, S. Perrin, E. Quevarec, C. Fournie, S. Desgraupes, N. Arhel, I. Bribès, B. Gouy, J. Zoladek.

L’équipe en Mars 2022
De gauche à droite: N. Arhel, E. Arsac,S. Nisole, P. Gonin, A. Decorsière, M. Cartron, A. Vidal, A. Boulay, J. Zoladek, C. Chamontin.

L’équipe en Mars 2021
De gauche à droite: C. Chamontin, N. Arhel, S. Nisole, M.F. Martin, H. Abiven, G. Maarifi, J. Fernandez, P. Nouaux, E. Gerber-Tichet, A. Boulay, Q. Hertel, F. Blanchet.
Membres de l’équipe
 Nathalie Arhel – Directrice de Recherche CNRS
Nathalie Arhel – Directrice de Recherche CNRS
 Jim Zoladek – Chercheur CNRS
Jim Zoladek – Chercheur CNRS
 Sophie Desgraupes – Chercheuse post-doctorale, ANRS
Sophie Desgraupes – Chercheuse post-doctorale, ANRS
 Marion Cannac – Doctorante ENS de Lyon
Marion Cannac – Doctorante ENS de Lyon
Ils ont travaillé avec nous (VTRIS Alumni)
 Sébastien Nisole – Directeur de Recherche INSERM, 2017-2025
Sébastien Nisole – Directeur de Recherche INSERM, 2017-2025
 Inès Bribes – Doctorante, 2022-2025
Inès Bribes – Doctorante, 2022-2025
 Guillaume Beucher – Chercheur post-doctoral ANR, 2024-2025
Guillaume Beucher – Chercheur post-doctoral ANR, 2024-2025
 Adrien Decorsière – Chercheur CNRS, 2021-2025
Adrien Decorsière – Chercheur CNRS, 2021-2025
 Suzon Perrin – Assistante Ingénieure, 2024-2025
Suzon Perrin – Assistante Ingénieure, 2024-2025
 Maël Seite – Etudiant M2 (Université de Rennes), 2024
Maël Seite – Etudiant M2 (Université de Rennes), 2024
 Rokhaya Gaye – Etudiante M1 (Université de Montpellier), 2024
Rokhaya Gaye – Etudiante M1 (Université de Montpellier), 2024
 Maxime Gonzalez – Etudiant M1 (Université de Montpellier), 2024
Maxime Gonzalez – Etudiant M1 (Université de Montpellier), 2024
 Thomas Léocadie – Etudiant M2 (ENS Saclay), 2023
Thomas Léocadie – Etudiant M2 (ENS Saclay), 2023
 Emmanuel Quevarec – Etudiant M2 (ENSCM), 2023
Emmanuel Quevarec – Etudiant M2 (ENSCM), 2023
 Benoît Gouy – Etudiant M1 (ENS Lyon), 2023
Benoît Gouy – Etudiant M1 (ENS Lyon), 2023
 Soléna Rossi – Etudiante M1 (Université de Montpellier), 2023
Soléna Rossi – Etudiante M1 (Université de Montpellier), 2023
 Chloé Fournie – Etudiante M1 (Université de Montpellier), 2023
Chloé Fournie – Etudiante M1 (Université de Montpellier), 2023
 Célia Chamontin – Assistante Ingénieure (Université de Montpellier), 2017-2022
Célia Chamontin – Assistante Ingénieure (Université de Montpellier), 2017-2022
 Pauline Gonin, Etudiante M2 (Université de Montpellier), 2022
Pauline Gonin, Etudiante M2 (Université de Montpellier), 2022
 Mateo Cartron, Etudiant M2 (Université de Rennes), 2022
Mateo Cartron, Etudiant M2 (Université de Rennes), 2022
 Emma Arsac, Etudiante M2 (Université de Montpellier), 2022
Emma Arsac, Etudiante M2 (Université de Montpellier), 2022
 Amélie Vidal, Etudiante M1 (Université de Montpellier), 2022
Amélie Vidal, Etudiante M1 (Université de Montpellier), 2022
 Aude Boulay, Assistante Ingénieure, Sidaction, 2020-2022
Aude Boulay, Assistante Ingénieure, Sidaction, 2020-2022
 Ghizlane Maarifi, Postdoc ANRS, 2019-2021
Ghizlane Maarifi, Postdoc ANRS, 2019-2021
 Marie-France Martin, Doctorante CBS2 Montpellier, Labex EpiGenMed, 2018-2021
Marie-France Martin, Doctorante CBS2 Montpellier, Labex EpiGenMed, 2018-2021
 Fabien Blanchet, Chercheur INSERM, 2019-2022
Fabien Blanchet, Chercheur INSERM, 2019-2022
 Quentin Hertel, Doctorant CBS2 Montpellier, 2020-2022
Quentin Hertel, Doctorant CBS2 Montpellier, 2020-2022
 Camille Talercio, Etudiante M1 (Université de Montpellier), 2021-2022
Camille Talercio, Etudiante M1 (Université de Montpellier), 2021-2022
 Pierre Nouaux, Assistant Ingénieur, SATT AxLR, 2021
Pierre Nouaux, Assistant Ingénieur, SATT AxLR, 2021
 Elina Gerber-Tichet, Etudiante M2 (Université de Montpellier), 2021
Elina Gerber-Tichet, Etudiante M2 (Université de Montpellier), 2021
 Hervé Abiven, Etudiant 5e année (Ecole de Biologie Industrielle), 2021
Hervé Abiven, Etudiant 5e année (Ecole de Biologie Industrielle), 2021
 Juliette Fernandez, Doctorante Sidaction / Ingénieur d’études, SATT AxLR, 2017-2021
Juliette Fernandez, Doctorante Sidaction / Ingénieur d’études, SATT AxLR, 2017-2021
 Sarah Maillet, Doctorante, ANRS, 2017-2020
Sarah Maillet, Doctorante, ANRS, 2017-2020
 Carla Alemany, Etudiante L3 (Université de Montpellier), 2020
Carla Alemany, Etudiante L3 (Université de Montpellier), 2020
 Lina Lapeyre, Etudiante M2 (Université de Montpellier), 2020
Lina Lapeyre, Etudiante M2 (Université de Montpellier), 2020
 Anne-Claire Aurilio, Etudiante M1 (Université de Montpellier), 2019-2020
Anne-Claire Aurilio, Etudiante M1 (Université de Montpellier), 2019-2020
 Justine Lagisquet, IE Recherche, 2017-2019
Justine Lagisquet, IE Recherche, 2017-2019
 Willy Lutz, Etudiant L3 (Université de Nîmes), 2019
Willy Lutz, Etudiant L3 (Université de Nîmes), 2019
 Richard de Reuver, Etudiant M2 Erasmus (Leiden University, Pays-Bas), 2018
Richard de Reuver, Etudiant M2 Erasmus (Leiden University, Pays-Bas), 2018
 Samah Sharif, Etudiante M1 (Université de Montpellier), 2018
Samah Sharif, Etudiante M1 (Université de Montpellier), 2018
 Abderezak Zebboudj, Postdoc, 2017-2018
Abderezak Zebboudj, Postdoc, 2017-2018
PUBLICATIONS 2015-2023
2026
– Desgraupes S, Boireau S, Khalil M, Aouinti S, Nisole S, Bolloré K, Barbaria W, Barzaghi F, Dilena R, Boon M, Lunsing RJ, Tuaillon E, Westerholm-Ormio M, Deiva K, Bakker DP, Kuijpers TW, Yeh EA, Lim M, Picot MC, Meyer P, Arhel NJ. An Inflammatory Signature Associated with Genetic 1 Predisposition to Acute Necrotizing Encephalopathy. medRxiv 2026.04.24.26350762.
– Desgraupes S, Decorsière A, Perrin S, Gouy B, Wang YE, Palazzo AF, Munier S, Arhel NJ. The genetic driver of Acute Necrotizing Encephalopathy, RANBP2, regulates the inflammatory response to Influenza A virus infection. Nat Commun. 2026 Feb 6.
– Medkour H, Bocci F, Schneider N, Serrato-Pomar I, Rey-Cadilhac F, Miot EF, Saron W, St John A, Maarifi G, Liu Y, Missé D, Nie Q, Smith DR, Nisole S, Plikus MV, Pompon J. Single-cell characterization of skin response to a bite by West Nile virus-infected mosquito reveals fibroblast-mediated barrier to transmission. bioRxiv 2026.01.08.698384
2025
– Leplat M, Desgraupes S, Beucher G, Decorsière A, Perrin A, Perrin S, Arhel NJ. ANEmone : la 1re conférence Science & Familles sur l’encéphalopathie nécrosante aiguë suscite l’espoir pour une maladie génétique ultra-rare. Virologie. 2025, 29(6):431-434.
– Cannac M, Zoladek J, Bribes I, Fresneau–Resende M, Legrand A, Demeure R, Zusinaite E, Merits A, Etienne L, Nisole S. SAMD9L inhibits flavivirus translation independently of its capacity to trigger innate immune response. PLoS Pathog. 2025, 21(12):e1013773.
– Bribes I, Nisole S. Zika Virus: A Tale of Two Lineages. Pathogens. 2025, 14(11):1151.
– Zoladek J, Cannac M, Seite M, Simonin Y, Wilson S, Nisole S. MITD1, an interferon-induced factor that inhibits the replication of neurotropic flaviviruses. Virologie. 2025, 29(5):376-377.
– Nisole S, Gilmer D. 2025 Renaud-Mahieux Awards. Virologie. 2025, 29(5):373.
– Hausdorff M, Delpal A, Machin H, Tahir A, Zoladek J, Gucciardi F, Swain J, Gros N, Muriaux D, Nisole S, Canard B, Vasseur JJ, Decroly E, Debart F. Synthesis and in vitro inhibitory activity of N-arylsulfonamide adenosine analogues designed to target SARS-CoV-2 nsp14 N7-methyltransferase. Bioorg Chem. 2025, 166: 109104
– Desgraupes S, Arhel N. Unravelling the diversity of RANBP2: protein isoforms and implications for cellular function and human disease. J Mol Biol. 2025, 437(24):169452.
– Zoladek J, Cannac M, Nisole S. MITD1 inhibits the replication of neurotropic flaviviruses in microglial cells. Med Sci. 2025, 41:640–642.
– Bribes I, Zoladek J, Cannac M, Salinas S, Wilson SJ, Nisole S. African strains of Zika virus resist ISG-mediated restriction. PLoS Negl Trop Dis. 2025, 19(7):e0013326.
– Arhel NJ. Fostering better science by releasing biomedical research and innovation from the grip of rich nations. PLOS Glob Public Health. 2025, 5(6):e0004709.
– Medkour H, Pruvost L, Miot EF, Gong X, Vaissayre V, Tavadia M, Boutinaud P, Revel J, Hitakarun A, Sornjai W, Zoladek J, Duncan Smith R, Nisole S, Nolte-‘t Hoen E, Bertrand-Michel J, Missé D, Marti G, Pompon J. Sphingomyelins in mosquito saliva reconfigure skin lipidome to promote viral protein levels and enhance transmission of flaviviruses. Cell Metab. 2025, S1550-4131(25)00295-5.
– Zoladek J, Cannac M, Seite M, Davies E, Quellec J, Barthelemy J, Gorna K, Desgraupes S, Bribes I, Salinas S, Coulpier M, Arhel NJ, Palmarini M, Simonin Y, Wilson SJ, Nisole S. MITD1 is a brain-specific interferon-inducible factor that inhibits flavivirus replication. Proc Natl Acad Sci U S A. 2025, 122(12):e2502064122.
– Zoladek J, Deymier S, Cimarelli A, Nisole S. Not all RNAs are created equal for the antiviral RNase ISG20. Trends Microbiol. 2025, 33(6):583-585.
– Serrato-Pomar I, Zoladek J, Medkour H, Narpon Q, Rey-Cadilhac F, Rossi S, French S, Modahl C, Sornjai W, Miot E, Hamel Rn Medianikov O, Missé D, Nisole S, Pompon J. Multiple flaviviruses secrete a viral non-coding RNA in mosquito salivary vesicles to enhance saliva infectivity by reducing early IFN response. BioRxiv. 2025.01.21.634113.
2024
– Zoladek J, Caval V, Paillart JC, Decroly E, Nisole S. How Usutu virus resists ISG20-mediated restriction. Med Sci. 2024, 40(12):973-975.
– Bekaddour N, Smith N, Caspar B, Grinberg S, Giorgiutti S, Rodeschini V, Dupuy S, Leboulanger N, Duffy D, Soulas-Sprauel P, Gies V, Korganow AS, Nisole S, Herbeuval JP. The histamine analogue clobenpropit modulates IRF7 phosphorylation and interferon production by targeting CXCR4 in systemic lupus erythematosus models. Front. Immunol. 2024, 15:1490593.
– Zoladek J, El Kazzi P, Caval V, Vivet-Boudou V, Cannac M, Davies EL, Rossi S, Bribes I, Rouilly L, Simonin Y, Jouvenet N, Decroly E, Paillart JC, Wilson SJ, Nisole S. A specific domain within the 3′ untranslated region of Usutu virus confers resistance to the exonuclease ISG20. Nat Commun. 2024, 2;15(1):8528.
– Boulay A, Quevarec E, Malet I, Nicastro G, Chamontin C, Perrin S, Henriquet C, Pugnière M, Courgnaud V, Blaise M, Marcelin AG, Taylor IA, Chaloin L, Arhel NJ. A new class of capsid-targeting inhibitors that specifically block HIV-1 nuclear import. EMBO Mol Med. 2024, 16(11):2918-45.
– Quellec J, Piro-Megy C, Cannac M, Nisole S, Marty FH, Gosselet F, Shimizu F, Kanda T, Cêtre-Sossah C, Salinas S. Rift Valley fever virus is able to cross the human blood-brain barrier in vitro by direct infection with no deleterious effects. J Virol. 2024.
– Nisole S. 2024: The Olympic Games go viral. Virologie. 2024, 28 (5):301-303.
– Cannac M, Nisole S. TRIMming down Flavivirus Infections. Viruses. 2024, 16(8):1262.
– Medkour H, Pruvost L, Gong X, Vaissayre V, Boutinaud P, Revel J, Hitakarun A, Sornjai W, Zoladek J, Smith DR, Nisole S, Nolte-t Hoen E, Bertrand-Michel J, Missé D, Marti G, Pompon J. Sphingomyelins in mosquito saliva modify the host lipidome to enhance transmission of flaviviruses by promoting viral protein levels. BioRxiv. 2024.06.14.599058.
– Decombe A, El Kazzi P, Nisole S, Decroly E. How do 2′-O-methylations within Human Immunodeficiency Virus type 1 (HIV-1) genome regulate its replication? Med Sci. 2024, 40(5):421-427.
– Decombe A, Peersen O, Sutto-Ortiz P, Chamontin C, Piorkowski G, Canard B, Nisole S, Decroly E. Internal RNA 2′-O-methylation on the HIV-1 genome impairs reverse transcription. Nucleic Acids Res. 2024, 52(3):1359-1373.
– Vouillon A, Barthelemy J, Lebeau L, Nisole S, Savini G, Lévêque N, Simonin Y, Garcia M, Bodet C. Skin tropism during Usutu virus and West Nile virus infection: an amplifying and immunological role. J Virol. 2024, 98(1):e0183023.
2023
– Gouy B, Decorsière A, Desgraupes S, Duan W, Ouyang H, Wang YE, Yeh EA, Palazzo AF, Moraes TJ, Nisole S, Arhel NJ. Rapid and inexpensive bedside diagnosis of RAN binding protein 2-associated acute necrotizing encephalopathy. Front. Neurol. 2023, 14:1282059.
– Zoladek J and Nisole S. Mosquito-borne flaviviruses and type I interferon: catch me if you can! Front. Microbiol. 2023, 14:1257024.
– Arhel NJ, Field MC. Biomedical implications of nuclear transport. FEBS Lett. 2023, 597(20):2499-2500.
– Desgraupes S, Etienne L, Arhel NJ. RANBP2 evolution and human disease. FEBS Lett. 2023, 597(20):2519-2533.
– Bekaddour N, Smith N, Beitz B, Llibre A, Dott T, Baudry A, Korganow AS, Nisole S, Mouy R, Breton S, Bader-meunier B, Duffy D, Terrier B, Schneider B, Quartier P, Rodero MP, Herbeuval JP. Targeting the chemokine receptor CXCR4 with histamine analog to reduce inflammation in juvenile arthritis. Front. Immunol. 2023, 14:1178172.
– Nisole S, Gilmer D. Prix Renaud-Mahieux – XXVes JFV. Virologie. 2023, 27(3):203.
– Zoladek J, Cannac M, Cartron M, Léocadie T, Wilson SJ, Nisole S. Identification de facteurs cellulaires interférant avec la réplication des virus West Nile et Usutu. Virologie. 2023, 27(3):204-205.
– Boulay A, Trabanelli S, Boireau S, Boyer-Clavel M, Nisole S, Romero P, Jandus C, Beignon AS, Arhel NJ. Assessing the Impact of Persistent HIV Infection on Innate Lymphoid Cells Using In Vitro Models. Immunohorizons. 2023, 7(3):243-255.
– El Kazzi P, Rabah N, Chamontin C, Poulain L, Ferron F, Debart F, Canard B, Missé D, Coutard B, Nisole S, Decroly E. Internal RNA 2’O-methylation in the HIV-1 genome counteracts ISG20 nuclease-mediated antiviral effect. Nucleic Acids Research, 2023, 51(6):2501-2515.
– Constant O, Maarifi G, Barthelemy J, Martin MF, Tinto B, Savini G, Van de Perre P, Nisole S, Simonin Y, Salinas S. Differential effects of Usutu and West Nile viruses on neuroinflammation, immune cell recruitment and blood brain barrier integrity. Emerg Microbes Infect. 2023, 12(1):2156815.
2022
– Vitour D, Nisole S, Lévêque N, Saulnier A, Tordo N, Gatignol A, Gilmer D. Une année dans Virologie : des virus persistent, d’autres émergent. Virologie. 2022, 26(6):405-408.
– Pompon J, Nisole S. Comment les flavivirus nous assaisonnent pour appâter les moustiques. Virologie. 2022, 26(4):315-317.
– Maarifi G, Martin MF, Zebboudj A, Boulay A, Nouaux P, Fernandez J, Lagisquet J, Garcin D, Gaudin R, Arhel NJ#, Nisole S#. Identifying enhancers of innate immune signaling as broad-spectrum antivirals active against emerging viruses. Cell Chem Biol. 2022, 29(7):1113-1125.
– Mac Kain A*, Maarifi G*, Aicher SM, Arhel NJ, Baidaliuk A, Munier S, Donati F, Vallet T, Tran QD, Hardy A, Chazal M, Porrot F, OhAinle M, Carlson-Stevermer J, Oki J, Holden K, Zimmer G, Simon-Lorière E, Bruel T, Schwartz O, van der Werf S, Jouvenet N#, Nisole S#, Vignuzzi M#, Roesch F#. Identification of DAXX as a restriction factor of SARS-CoV-2 through a CRISPR/Cas9 screen. Nat Commun. 2022, 13(1):2442.
– Martin MF, Maarifi G, Abiven H, Seffals M, Mouchet N, Beck C, Bodet C, Lévèque N, Arhel NJ, Blanchet FP, Simonin Y, Nisole S. Usutu Virus escapes langerin-induced restriction to productively infect human Langerhans cells, unlike West Nile virus. Emerg Microbes Infect. 2022, 11(1):761-774.
2021
– Chamontin C, Bossis G, Nisole S, Arhel NJ, Maarifi G. Regulation of viral restriction by post-translational modifications. Viruses. 2021, 13: 2197.
– Bekaddour N, Smith N, Beitz B, Llibre A, Dott T, Baudry A, Korganow AS, Nisole S, Mouy R, Breton S, Bader-Meunier B, Duffy D, Terrier B, Schneider B, Quartier P, Rodero M, Herbeuval JP. Targeting the chemokine receptor CXCR4 with histamine analogue to reduce inflammation in juvenile arthritis: a proof of concept for COVID-19 therapeutic approach. BioRxiv, 2021.10.24.465080.
– Sonigo P, Petit C, Arhel NJ. Faut-il vacciner contre la détection par PCR ou contre la maladie Covid-19 ? Virologie. 2021 Oct 12.
– Martin MF, Maarifi G, Abiven H, Seffals M, Mouchet N, Beck C, Bodet C, Lévêque N, Arhel NJ, Blanchet FP, Simonin Y, Nisole S. Usutu virus uses langerin as a receptor to productively infect Langerhans cells more efficiently than West Nile virus. BioRxiv, 2021.08.17.456611.
– Arone C, Dibsy R, Inamdar K, Lyonnais S, Arhel NJ, Favard C, Muriaux D. Illuminating the nanoscopic world of viruses by fluorescence super-resolution microscopy. Virologie. 2021, 25(3):47-60.
– Maarifi G, Lagisquet J, Hertel Q, Bonaventure B, Chamontin C, Fuchs K, Moncorgé O, Tauziet M, Mombled M, Papin L, Molès JP, Bodet C, Lévèque N, Gross A, Arhel N, Nisole S, Van de Perre P, Goujon C, Blanchet FP. Alarmin S100A9 restricts retroviral infection by limiting reverse transcription in human dendritic cells. EMBO J. 2021, 40(16):e106540.
– Arhel NJ. An unprecedented interest for the human immunodeficiency virus capsid. Med Sci. 2021, 37(5):549-552.
– Mac Kain A, Maarifi G, Aicher SM, Arhel NJ, Baidaliuk A, Vallet T, Tran QD, Hardy A, Chazal M, Porrot F, OhAinle M, Carlson-Stevermer J, Oki J, Holden K, Simon-Loriere E, Bruel T, Schwartz O, Jouvenet N, Nisole S, Vignuzzi M, Roesch F. Identification of DAXX as a restriction factor of SARS-CoV-2 through a CRISPR/Cas9 screen. BioRxiv, 2021.05.06.442916.
– Gosselin-Grenet AS, Servan de Almeida R, Roumagnac P, Ayouba A, Simonin Y, Nisole S. Virus et chercheurs sous le soleil de Montpellier. Virologie. 2021, 25(S1):3-5.
– Rebendenne A, Valadão ALC, Tauziet M, Maarifi G, Bonaventure B, McKellar J, Planès R, Nisole S, Arnaud-Arnould M, Moncorgé O, Goujon C. SARS-CoV-2 triggers an MDA-5-dependent interferon response which is unable to control replication in lung epithelial cells. J Virol. 2021, JVI.02415-20.
– Fernandez J, Hassen-Khodja C, Georget V, Rose T, Jacob Y, Janin YL, Nisole S, Vidalain PO, Arhel NJ. Measuring the subcellular compartmentalization of viral infections by protein complementation assay. PNAS 2021, 118(2):e2010524118.
2020
– Volcic M, Sparrer KMJ, Koepke L, Hotter D, Sauter D, Stürzel CM, Scherer M, Stamminger T, Hofmann TG, Arhel NJ, Wiesmüller L, Kirchhoff F. Vpu modulates DNA repair to suppress innate sensing and hyper-integration of HIV-1. Nat Microbiol. 2020, 5(10):1247-1261.
– Arhel NJ. Early HIV replication revisited. Nat Microbiol. 2020, 5(9):1065-1066.
– Clé M, Desmetz C, Barthelemy J, Martin MF, Constant O, Maarifi G, Foulongne V, Bolloré K, Glasson Y, De Bock F, Blaquiere M, Dehouck L, Pirot N, Tuaillon E, Nisole S, Najioullah F, Van de Perre P, Cabié A, Marchi N, Gosselet F, Simonin Y, Salinas S. Zika Virus Infection Promotes Local Inflammation, Cell Adhesion Molecule Upregulation, and Leukocyte Recruitment at the Blood-Brain Barrier. mBio. 2020, 11(4):e01183-20.
– Sa Ribero M, Jouvenet N, Dreux M, Nisole S. Interplay between SARS-CoV-2 and the type I interferon response. PLoS Pathog. 2020, 16(7):e1008737.
– Nisole S, Saulnier A, Gatignol A. Severe acute respiratory syndrome coronavirus 2 (SARS-CoV-2): Should we target the virus, the cell or the disease? Virologie. 2020, 24(3):135-141.
– Maillet S, Fernandez J, Decourcelle M, El Koulali K, Blanchet FP, Arhel NJ, Maarifi G, Nisole S. Daxx inhibits HIV-1 reverse transcription and uncoating in a SUMO-dependent manner. Viruses. 2020, 12(6):E636.
– Burette M, Allombert J, Lambou K, Maarifi G, Nisole S, Di Russo Case E, Blanchet FP, Hassen-Khodja C, Cabantous S, Samuel J, Martinez E, Bonazzi M. Modulation of innate immune signaling by a Coxiella burnetii eukaryotic-like effector protein. PNAS 2020, 117(24):13708-13718.
– Fernandez J, Arhel NJ. HIV capsid and productive infection: taking steps in the right direction. Virologie. 2020, 24(2):88-98.
– Maarifi G, Czubala MA, Lagisquet J, Ivory MO, Fuchs K, Papin L, Birchall JC, Nisole S, Piguet V, Blanchet FP. Langerin (CD207) represents a novel interferon-stimulated gene in Langerhans cells. Cell Mol Immunol. 2020, 17(5):547-549.
– Martin MF, Nisole S. West Nile Virus restriction in mosquito and human cells: A virus under confinement. Vaccines. 2020, 8(2):E256.
– Maarifi G, Smith N, Nisole S. Interferon response: with great power comes great responsibility? Med Sci. 2020, 36(3):206-209.
– Hayek S, Pietrancosta N, Hovhannisyan AA, Alves de Sousa R, Bekaddour N, Ermellino L, Tramontano E, Arnould S, Sardet C, Dairou J, Diaz O, Lotteau V, Nisole S, Melikyan G, Herbeuval JP, Vidalain PO. Cerpegin-derived furo[3,4-c]pyridine-3,4(1H,5H)-diones enhance cellular response to interferons by de novo pyrimidine biosynthesis inhibition. Eur J Med Chem. 2020, 186:111855.
– Fernandez J, Arhel NJ. Transportin-1 orchestrates HIV-1 uncoating and nuclear entry. Med Sci. 2020, 36(3):203-206.
2019
– Salinas S, Simonin Y, L’Ambert G, Nisole S. Autochthonous cases of Zika virus in metropolitan France: a new paradigm for this arbovirus? Virologie. 2019, 23(6):329-332.
– Maarifi G, Smith N, Maillet S, Moncorgé O, Chamontin C, Edouard J, Sohm F, Blanchet FP, Herbeuval JP, Lutfalla G, Levraud JP, Arhel NJ, Nisole S. TRIM8 is required for virus-induced IFN response in human plasmacytoid dendritic cells. Sci Adv. 2019, 5(11):eaax3511.
– Fernandez J, Machado AK, Lyonnais S, Chamontin C, Gärtner K, Léger T, Henriquet C, Garcia C, Portilho DM, Pugnière M, Chaloin L, Muriaux D, Yamauchi Y, Blaise M, Nisole S, Arhel NJ. Transportin-1 binds to the HIV-1 capsid via a nuclear localization signal and triggers uncoating. Nat Microbiol. 2019 4(11):1840-1850.
– Smith N, Rodero MP, Bekaddour N, Bondet V, Ruiz-Blanco YB, Harms M, Mayer B, Badder-Meunier B, Quartier P, Bodemer C, Baudouin V, Dieudonné Y, Kirchhoff F, Garcia ES, Charbit B, Leboulanger N, Jahrsdörfer B, Richard Y, Korganow AS, Münch J, Nisole S, Duffy D and Herbeuval JP. Control of TLR7-mediated type I IFN signaling in pDCs through CXCR4 engagement—A new target for lupus treatment. Science Advances. 2019, 5(7):eaav9019.
– Hayek S, Bekaddour N, Besson L, Alves de Sousa R, Pietrancosta N, Viel S, Smith N, Jacob Y, Nisole S, Mandal R, Wishart DS, Walzer T, Herbeuval JP, Vidalain PO. Identification of primary natural killer cell modulators by chemical library screening with a luciferase based functional assay. SLAS Discovery. 2019, 24(1):25-37.
– Nisole S, Fernandez J, Maarifi G, Arhel NJ. SUMO regulates the capacity of TRIM5α to inhibit HIV-1. Med Sci. 2019, 35(2):106-109.
2018
– Maarifi G, Fernandez J, Portilho DM, Boulay A, Dutrieux J, Oddos S, Butler-Browne G, Nisole S, Arhel NJ. RanBP2 regulates the anti-retroviral activity of TRIM5α by SUMOylation at a predicted phosphorylated SUMOylation motif. Commun Biol. 2018, 1:193.
– Nisole S. Usutu, that which does not kill us makes us stronger. Virologie. 2018, 22(5):231-2.
2017
– Lucas-Hourani M, Dauzonne D, Mulier-Lehmann H, Khiar S, Nisole S, Dairou J, Helynck O, Afonso P, Tangy F, Vidalain PO. An original chemical series of pyrimidine biosynthesis inhibitors that boost the antiviral interferon response. Antimicrob. Agents Chemother. 2017, 61(10): e00383-17.
– Khiar S, Lucas-Hourani M, Nisole S, Smith N, Helynck O, Bourgine M, Ruffié C, Herbeuval JP, Munier-Lehmann H, Tangy F, Vidalain PO. Identification of a small molecule that primes the type I interferon response to cytosolic DNA. Sci Rep. 2017, 7(1):2561.
– Smith N, Pietrancosta N, Davidson S, Dutrieux J, Chauveau L, Cutolo P, Dy M, Scott-Algara D, Manoury B, Zirafi O, McCort-Tranchepain I, Durroux T, Bachelerie F, Schwartz O, Münch J, Wack A, Nisole S, Herbeuval JP. Natural amines inhibit activation of human plasmacytoid dendritic cells through CXCR4 engagement. Nat Commun. 2017, 8:14253.
2016
– Smith N, Vidalain PO, Nisole S, Herbeuval JP. An efficient method for gene silencing in human primary plasmacytoid dendritic cells: silencing of the TLR7/IRF 7 pathway as a proof of concept. Sci Rep. 2016, 6:29891.
– Maarifi G, Hannoun Z, Geoffroy MC, El Asmi F, Zarrouk K, Nisole S, Blondel D, Chelbi-Alix M. MxA mediates SUMO-induced resistance to Vesicular Stomatitis Virus. J Virol. 2016, 90(14):6598-610.
– Portilho DM, Fernandez J, Ringeard M, Machado AK, Boulay A, Mayer M, Müller-Trutwin M, Beignon AS, Kirchhoff F, Nisole S, Arhel NJ. Endogenous TRIM5α function is regulated by SUMOylation and nuclear sequestration for efficient innate sensing in dendritic cells. Cell Reports. 2016, 14(2):355-69.
– Portilho DM, Persson R, Arhel N. Role of non-motile microtubule-associated proteins in virus trafficking. Biomol Concepts. 2016, 7(5-6):283-292.
– Maillet S, Nisole S. Daxx, a broad-spectrum viral restriction factor. Virologie, 2016, 20(5):261-72.
– Maarifi G, Dianoux L, Nisole S, Chelbi-Alix MK. SUMO paralogs and interferon response. Med Sci. 2016, 32(2):141-3.
2015
– Dutrieux J, Maarifi G, Portilho DM, Arhel NJ, Chelbi-Alix MK, Nisole S. PML/TRIM19-dependent inhibition of retroviral reverse-transcription by Daxx. PLoS Pathog. 2015, 11(11):e1005280.
– Fernandez J, Portilho DM, Danckaert A, Munier S, Becker A, Roux P, Zambo A, Shorte S, Jacob Y, Vidalain PO, Charneau P, Clavel F, Arhel NJ. Microtubule-associated proteins 1 (MAP1) promote human immunodeficiency virus type I (HIV-1) intracytoplasmic routing to the nucleus. J Biol Chem. 2015, 290(8):4631-46.
– Maarifi G, Maroui MA, Dutrieux J, Dianoux L, Nisole S, Chelbi-Alix MK. SUMO promotes resistance to interferon. J Immunol. 2015, 195(5):2312-24.
– Dutrieux J, Portilho DM, Arhel NJ, Hazan U, Nisole S. TRIM5α is a SUMO substrate. Retrovirology. 2015, 12:28.
– Brantis-de-Carvalho CE, Maarifi G, Gonçalves Boldrin PE, Zanelli CF, Nisole S, Chelbi-Alix MK, Valentini SR. MxA interacts with and is modified by the SUMOylation machinery. Exp Cell Res. 2015, 330(1):151-63.
– Kotera N, Dubost E, Milanole G, Doris E, Gravel E, Arhel N, Brotin T, Dutasta JP, Cochrane J, Mari E, Boutin C, Léonce E, Berthault P, Rousseau B. A doubly responsive probe for the detection of Cys4-tagged proteins. Chem Commun. 2015, 51(57):11482-4.
– Blondel D, Maarifi G, Nisole S, Chelbi-Alix M. Resistance to Rhabdoviridae Infection and Subversion of Antiviral Responses. Viruses. 2015, 7:3675-702.
– Octobre 2025: L’équipe VTRIS est fière d’annoncer que Jim Zoladek a été recruté comme chercheur au CNRS !
Félicitations Jim 🎉 Nous te souhaitons plein de succès dans cette nouvelle aventure !

– Septembre 2025: Pour sa dernière participation, l’équipe VTRIS remporte une nouvelle fois la Pipette d’Or !

– Juillet 2025: Nathalie Arhel et Sébastien Nisole, ambassadeurs de l’équipe VTRIS au congrès ASV 2025 à Montréal.

– Avril 2025: L’équipe VTRIS aux Journées Francophones de Virologie 2025, à l’ENS Lyon.

De gauche à droite : Sophie Desgraupes présente ses travaux sur le rôle de RanBP2 dans l’encéphalopathie nécrosante aiguë 1 (ANE1), Marion Cannac sur l’inhibition de la traduction des flavivirus par la protéine SAMD9L, et Jim Zoladek reçoit à nouveau le Renaud Mahieux Award pour son poster sur le rôle de MITD1 dans la protection des microglies contre les virus neurotropes.
– Novembre 2024: L’équipe VTRIS sous les feux de la rampe au Montpellier Infection & Immunity Meeting!

A gauche: Jim Zoladek sur scène pour présenter ses derniers travaux sur la restriction des flavivirus dans les cellules microgliales. A droite: Inès Bribes et Marion Cannac reçoivent respectivement le prix de la meilleure présentation orale et du meilleur poster. Bien joué, l’équipe!!
– Octobre 2024: Quelle était la probabilité que 2 articles de l’équipe sortent le même jour ?

– Avril 2024: L’équipe VTRIS à Bruxelles, pour les Journées Francophones de Virologie.
 Gauche: Sophie Desgraupes présente son poster sur le rôle de la nucléoporine RanBP2 dans la régulation de l’export nucléaire du virus de la grippe. Droite: Jim Zoladek expose son travail sur la susceptibilité des flavivirus à l’exonucléase ISG20.
Gauche: Sophie Desgraupes présente son poster sur le rôle de la nucléoporine RanBP2 dans la régulation de l’export nucléaire du virus de la grippe. Droite: Jim Zoladek expose son travail sur la susceptibilité des flavivirus à l’exonucléase ISG20.
– Novembre 2023: VTRIS @ Singapour !
 Gauche: Nathalie Arhel donne un séminaire sur « Le rôle des pores nucléaires dans l’infection et l’immunité » au laboratoire A*STAR Infectious Diseases (ID Labs). Droite: Sébastien Nisole remporte le prix de la meilleure présentation orale à l’International Vector-borne Diseases Conference (IVBDC).
Gauche: Nathalie Arhel donne un séminaire sur « Le rôle des pores nucléaires dans l’infection et l’immunité » au laboratoire A*STAR Infectious Diseases (ID Labs). Droite: Sébastien Nisole remporte le prix de la meilleure présentation orale à l’International Vector-borne Diseases Conference (IVBDC).
– Avril 2023: Jim Zoladek reçoit le prix Renaud Mahieux au cours des Journées Francophones de Virologie 2023, à l’Institut Pasteur.

– Avril 2023: L’équipe VTRIS à l’assaut du pic Saint-Loup!

– Février 2023: Sébastien Nisole au Symposium “The TRIM family meets in Montpellier”.

– Décembre 2022: Célébration de la promotion de Célia Chamontin avec les collègues.

– Septembre 2022: La pipette d’or revient enfin à la maison, après 3 ans d’absence!!
 « It came back to us… our own, our precious!! »
« It came back to us… our own, our precious!! »
L’équipe VTRIS remporte le challenge inter-équipes 2022 de l’IRIM avec cette photo:

– Août 2022 : Comment les moustiques nous piquent (et les conséquences) dans « The Conversation ».
– Juillet 2022: Postdoc à pourvoir dans l’équipe!

– Juin 2022: Notre papier récemment publié dans Cell Chem Biol (voir précédent post) a été présenté dans « This Week In Virology »!!

Cliquez ci-dessous pour voir Vincent Racaniello et ses co-animateurs expliquer notre article et la technologie Alpha Centauri (à partir de 39’55 ») : 
– Juin 2022: Encore un triple combo pour l’équipe VTRIS, qui publie 3 papiers coup sur coup!
- Maarifi G et al. Identifying enhancers of innate immune signaling as broad-spectrum antivirals active against emerging viruses. Cell Chem Biol (2022).
- Mac Kain A et al. Identification of DAXX as a restriction factor of SARS-CoV-2 through a CRISPR/Cas9 screen. Nat Commun (2022).
- Martin MF et al. Usutu Virus escapes langerin-induced restriction to productively infect human Langerhans cells, unlike West Nile virus. Emerg Microbes Infect (2022).

– Mars 2022: Nathalie Arhel présente ses derniers travaux lors de la Journée Scientifique de Sidaction, à l’Institut Pasteur.

– Mars 2022: Aujourd’hui, c’est Mardi-gras au labo!!

– Octobre 2021: On recrute!

– Avril 2021: On parle de notre projet de start-up, Alpha-Centauri, dans le Midi Libre.

– Mars 2021: Une belle matinée dans la garrigue.

– Novembre 2020: Après une brillante visio-soutenance, Sarah Maillet se voit décerner le titre de Docteur! Bravo Sarah!!

– Juillet 2020: Quentin Hertel décroche une bourse de thèse au concours de l’école doctorale CBS2. Bien joué, Quentin!! Nous sommes ravis que tu restes 3 ans de plus dans l’équipe!

– Juin 2020: Un grand merci à l’ANR et la Région Occitanie de financer notre projet Alpha-CoV, qui vise à mettre en œuvre un test rapide et fiable pour le criblage haut-débit de molécules antivirales actives contre le SARS-CoV-2.

– Mars/Avril 2020: L’équipe VTRIS garde le contact malgré le confinement.
– Février 2020: Juliette Fernandez reçoit le trophée i-PhD 2019 des mains de Frédérique Vidal, Ministre de l’Enseignement supérieur, de la Recherche et de l’Innovation. Félicitations, Juliette !!
 Les 29 lauréats du trophée i-PhD
Les 29 lauréats du trophée i-PhD
– Février 2020: Nathalie Arhel et Sébastien Nisole participent au congrès « Viruses – Novel Concepts in Virology » à Barcelone.
 Pouvez vous nous trouver?
Pouvez vous nous trouver?
 Nathalie préside la session « Viral genetics and evolution »
Nathalie préside la session « Viral genetics and evolution »
– Novembre 2019: Un grand bravo à notre nouveau Dr, Juliette Fernandez, qui a brillamment défendu sa thèse! On est tous fiers de toi, Juliette!

– Octobre 2019: Sébastien Nisole est éditeur invité d’un numéro spécial du journal Viruses intitulé « Facteurs antiviraux intrinsèques ». Les soumissions sont maintenant ouvertes et nous attendons vos contributions!
Date limite de soumission: 1er novembre 2020
Pour de plus amples informations, merci de visiter la page web dédiée à ce numéro:
https://www.mdpi.com/journal/viruses/special_issues/antiviral_factors

– Septembre 2019: Après 3 ans d’efforts, la très convoitée pipette d’or est enfin à nous…!!!
« It came to us, our own, our love… our precioussss!! »

L’équipe VTRIS remporte le challenge inter-équipes 2019 de l’IRIM avec cette photo:

Le Making-of:

– Septembre 2019: Ce n’est pas 1, ni 2, mais bien 3 papiers de l’équipe VTRIS qui viennent d’être acceptés pour publication… super rentrée!!

– Juillet 2019: Sarah Maillet, Célia Chamontin et Juliette Fernandez participent aux défis sportifs organisés pour les 80 ans du CNRS, au sein de l’équipe dIRIM Team!

– Mars 2019: L’IRIM arrive en force aux Journées Francophones de Virologie, à l’ENS Lyon. Juliette Fernandez y présente les travaux de l’équipe sur le rôle de TNPO1 dans le désassemblage et l’import nucléaire du VIH-1.

– Mars 2019: Nathalie Arhel, Célia Chamontin et Sébastien Nisole se joignent à l’équipe « IRIM Greyhound » pour le marathon de Montpellier en relais! 42,2km en 3h53… bien joué les lévriers!!

– Janvier 2019: Sitôt arrivé, sitôt financé! Fabien Blanchet vient d’obtenir un financement auprès de l’ANRS pour poursuivre son projet de recherche sur la restriction du VIH-1 dans les cellules de Langerhans. Bien joué, Fabien!!

– Décembre 2018: Nous sommes ravis d’accueillir un nouveau PI dans l’équipe, Fabien Blanchet, CR INSERM et spécialiste des cellules myeloïdes, de l’immunité antivirale et du VIH. Il nous rejoint accompagné de Ghizlane Maarifi, post-doc financée par l’ANRS. Nous leur souhaitons une chaleureuse bienvenue!

– Décembre 2018: Nathalie Arhel et Sébastien Nisole participent au congrès « Immunotherapies for Infectious Diseases » organisé à Lyon.

– Octobre 2018: L’équipe VTRIS au concours « Top Chef » de l’IRIM.
 De gauche à droite: J. Fernandez, S. Maillet, G. Maarifi.
De gauche à droite: J. Fernandez, S. Maillet, G. Maarifi.
– Septembre 2018: Nathalie Arhel organise un workshop très stimulant au Domaine de Verchant, avec le soutien de l’ANR.

– Juin 2018: Marie-France Martin obtient un financement de 3 ans auprès du Labex EpigenMed pour étudier la réponse immunitaire innée des arbovirus dans les cellules immunitaires humaines. Félicitations et bienvenue Marie-France!


– Mai 2018: Juliette Fernandez organise à l’IRIM, pour la première fois en région Occitanie, le congrès des Apprentis Chercheurs pour le compte de l’association l’Arbre des Connaissances. Des binômes de collégiens et lycéens ont eu l’opportunité de découvrir le travail en laboratoire tout au long de leur année scolaire et ont ensuite présenté leurs résultats devant leur famille et leurs professeurs lors d’un congrès organisé dans l’amphithéâtre du CNRS. Un grand merci aux équipes de l’IRIM qui ont accueilli ces chercheurs en herbe dans leur laboratoire.

– Avril 2018: Les membres de l’équipe VTRIS se joignent à la Team IRIM pour participer à la « Ruée des Fadas », une course d’obstacles de 8 km.

– Avril 2018: L’équipe acueille Richard de Reuver, étudiant hollandais en Master Erasmus, qui vient réaliser un stage de 6 mois. Bienvenue Richard!

– Février 2018: Nathalie Arhel et Sébastien Nisole participent au congès « Viruses – Breakthroughs in Viral Replication » à Barcelone.
 Qui nous trouvera sur ces photos?
Qui nous trouvera sur ces photos?
– Octobre 2017: l’équipe VTRIS remporte le 2e prix de la compétition vidéo de l’IRIM. Nous visons le premier prix pour la prochaine compétition, la très convoitée pipette d’or…!

 Photo de gauche, de gauche à droite: S. Maillet, J. Fernandez, C. Chamontin, A. Zebboudj, J. Lagisquet
Photo de gauche, de gauche à droite: S. Maillet, J. Fernandez, C. Chamontin, A. Zebboudj, J. Lagisquet
Photo de droite: S. Maillet et J. Fernandez
– Octobre 2017: L’équipe VTRIS est heureuse d’accueillir 2 nouveaux membres, Abderezak Zebboudj (postdoc) et Justine Lagisquet (Ingénieure d’Etudes). Bienvenue à Zak et Justine!

– Septembre 2017: Nous accueillons Célia Chamontin, qui rejoint l’équipe en temps qu’Assistante ingénieure statutaire (Université de Montpellier). Nous sommes ravis de ton arrivée dans l’équipe, Célia!

– Juin 2017: Sarah Maillet obtient un financement de 3 ans auprès de l’ANRS pour réaliser sa thèse au sein de l’équipe. Elle y étudiera le mécanisme moléculaire par lequel la protéine celulaire Daxx inhibe la rétro-transcription du VIH-1. Félicitations, Sarah!

– Mai 2017: Premier Escape game pour l’équipe VTRIS, qui parvient à sortir de la pièce en moins d’1 heure!
 De gauche à droite: S. Nisole, N. Arhel, C. Chamontin, J. Fernandez, S. Maillet
De gauche à droite: S. Nisole, N. Arhel, C. Chamontin, J. Fernandez, S. Maillet
– Avril 2017: L’équipe VTRIS participe à une chaîne humaine géante pour former le mot « Science » place du Peyrou à Montpellier. Nous sommes au niveau du 2e « C » de « Science » sur cette photo satellite.

– Mars 2017: Juliette Fernandez tient le stand Sidaction avec Véronique dans le hall de l’IRIM.

– Janvier 2017: Pendaison de crémaillère au laboratoire, pour célébrer la création de l’équipe avec le reste de l’Institut.

– Janvier 2017: Juliette Fernandez obtient un financement de 3 ans pour réaliser sa thèse au sein de l’équipe. Elle y développera des outils innovants pour étudier l’import nucléaire du VIH. Félicitations, Juliette!

– Janvier 2017: Inauguration de l’équipe Trafic viral, Restriction et Immunité innée (VTRIS en anglais, pour « Viral Trafficking, Restriction and Innate Signaling ») à l’IRIM.

EN BREF
L’équipe VTRIS a été créée au 1er janvier 2017, suite à un appel d’offres international lancé par l’IRIM. Elle bénéficie depuis sa création du soutien du labex EpiGenMed.

Financements









